فسفاته کردن با تسریع کننده های شیمیایی
ایجاد پوشش فسفاته را می توان به روش های شیمیایی ، مکانیکی یا الکتریکی تسریع کرد ولی اغلب از از عوامل شیمیایی که به نام تسریع کننده خوانده می شوند ، استفاده می شود . زیرا نتها باعث صرفه جویی در وقت می شوند بلکه می توان فرآیند را در دماهای کمتر یعنی 20 تا 25 درجه سانتی گراد انجام داد .

مواد اکسید کننده جزو مواد تسریع کننده های شیمیایی هستند ، از جمله این مواد می توان نیتراتها ، نیتریت ها و کلرات ها را نام برد . در محلول های فسفاته ، نیترات ها به صورت نیترات فلزات قلیایی یا نمک های روی و منگنز و یا در مخلوطی از نینرات یک فلز قلیایی و نیترات یک فلز سنگین ( روی و منگنز) به کار می روند . در حین فسفاته کردن در حضور آهن ، نیترات به نیتریت و یا به یک ترکیب نیترو احیا می شود. حال می تواند با هیدروژنی که بر اثر انحلال آهن توسط اسید فسفریک آزاد شده است واکنش دهد :
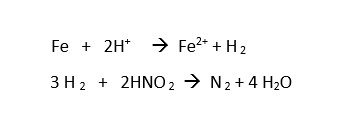
و می تواند فرو را به یون های فریک اکسید کند :

واکنش کلی اکسیداسیون به صورت زیر است :

نیتروژن تولید شده براثر احیای نیترات ، به عنوان یک گاز خنثی ، بر واکنش فسفاته کردن اثر معکوس ندارد. واکنش اخیر باعث ایجاد فسفات فریک غیر محلول می شود که به صورت لجن رسوب می کند ، درحالی که مقدار آهن موجود درحمام و در پوشش در حد مشخصی تثبیت می شود. اگر حمام خیلی خوب تجدید شود ، می تواند به طور تقریبا نامحدودی کار کند و پوشش های تقربیا یکنواخت با مقاومت به خوردگی ثابت تولید کند. وقتی دمای حمام 95 تا 98 درجه سانتی گراد باشد در حضور آهن و تصاعد هیدروژن ، نیتریت به شدت ناپایدار است از این رو سریعا تجزیه میشود و تجزیه محلول های حاوی تسریع کننده نیترات ، تنها مقدار بسیار کمی از نیتریت ها را نشان می دهد . به هر حال ، نیتیت به طور مداوم در نتیجه ی احیای نیترات تولید می شود . مقادیر بسیارکم از یون های مس ( 5-2 میلی گرم بر لیتر ) این احیا را تسریع می کنند. ( یون های مس به صورت اکسید کوپریک در پوشش رسوب می کنند . ) نیتریت حاصل برای اکسید کردن تمام یون های آهن II به آهن III ناکافی است. بنابراین ، مقدار معینی از یون های آهن II در محلول باقی می مانند ، اما به طور مطلوبی مقاومت به خوردگی پوشش حاصل را تحت تاثیر قرار می دهند . مشخص شده است که مقدار آهن در حمام های حاوی یون سدیم کمتر از حمام های بدون آن است . به جرات می توان گفت که این واقعییت تببین کننده تاثیر مطلوب یون های آهن روی اکسیداسیون NO به N2O توسط اکسیژن اتمسفر در حین دوره های توقف عملیات است ، زیرا تنها دی اکسید نیتروژن می تواند آهن را اکسید کند نه اکسید نیتروژن. مشخص است که در حین فسفاته کردن روی در محلول های حاوی تسریع کننده هیچ مقداری از یون های نیتریت و یون های آهن انباشته نمی شود و نسبت غلظت نیترات به No به سرعت بیش از واحد می شود . مقدار نیتریت تا 1 گرم بر لیتر افزایش یابد . بر اساس نظرمحقق جادون ، اکسید شدن آهن به دلیل وجود ترکیبات کمپلکس آهن است و نه نیترات و نه نیتریت هیچکدام به طور مستقیم آهن دو ظرفیتی را اکسید نمی کنند. عمل اکسید کنندگی نیترات ، به وضوح از حجم هیدروژن متصاعد شده در حین فسفاته کردن مشهود است . کمترین حجم هیدروژن از حمام فسفاته روی حاوی نیترات آزاد می شود. حجم گاز متصاعد شده از حمامی مشابه ، حاوی آهن اضافی تقریبا همان مقدار است اما گاز، حاوی مقدار بیشتری اکسید نیتروژن و اکسید هیدروژن است که به علت حضور یون های آهن II راحت تر تشکیل می شوند. مقدار گازمتصاعد شده از حمام فسفاته منگنزحاوی تسریع کننده نیترات ، تنها نصف مقدار گاز متصاعد شده از حمام بدون تسریع کننده است. زیرا زمان طولانی تری برای تشکیل پوشش در حمام بدون تسریع کننده لازم است . احتمالا عمل کاتالیزوری یون های روی برای تجزیه اسید نیتریک ، قوی تر از یون های منگنز است. انجمن کنتیننتال پارکر روش هایی را برای افزایش مصنوعی مقدار نیتریت در حمام فسفاته عرضه کرده است که این روش ها یا شامل افزودن مستقیم نیتریت به محلول است و یا کنترل مطلوب ترکیب حمام . افزودن نیترین موجب تشکیل مقدار بیشتری نیتریت از نیترات به طور خود کاتالیزوری می شود . نسبت زیاد نیتریت به فسفات در محلول 3:1 یا 2:1 برای تشکیل نیتریت مطلوب است و افزایش دما نیز همین اثر را دارد البته نمی توان دما را از دمای تجزیه نیتریت بیشتر کرد . در حمام های غلیظ ،مقدار کافی نیتریت حتی در کمتر از 80 درجه سانتی گراد می تواند تشکیل شود .اخیرا نیتراتها ف به تنهایی در محلول های حاوی فسفات های روی و کلسیم برای عملیات مقدماتی فولاد قبل از رسوب الکتروفورتیک پوشش های آلی تک لایه ای به کار می روند . مصرف نیتریت به همراه نیترات در حمام هایی با دمای اتاق کاربرد وسیعی دارد که بیشتر به صورت نمک فلزات قلیایی به کار می روند آما عیب آنها این است که در دماهای زیاد ناپایدارند . بر اساس تحقیقات سرعت تجزیه نیتریت در دمای فسفاته کردن 95 تا 98 درجه سانتی گراد به قدری زیاد است که قسمت اعظم نیتریت هدر می رود . از این رو جهت جلوگیری از مصرف بیش از حد موادشیمیایی و ایجاد شرایط بهداشتی کار ، مقدار نیتریت اضافه شده در حمام هایی با دمای زیاد باید کاملا متناسب انتخاب شود . ثابت تفکیک اسید نیترو وابسته به دماست ودر 0 درجه سانتی گراد برابر 0.602 و در 60 درجه سانتی گراد برابر 5130 است ، بنابر این نیتریت ها گاربرد وسیع تری در حمام های دما پایین دارند به ویژه در دمای اتاق . وقتی فولاد را در محلول های حاوی نیتریت سدیم فسفاته می کنند نسبت 1 به 1 NO و NO2 مداوما کم می شود ، زیرا دی اکسید تقریبا به طور کامل برای اکسیداسیون آهن دو ظرفیتی مصرف می شود و خود به نیتروژن احیا می شود. کلرات روی به صورت یک محلول آبی غلیظ که جذب کننده رطوبت است تغذیه می شود . کلرات ها عمدتا به صورت Zn( Clo3)2 مصرف می شوند. کلرات رو ی ب صورت یک محلول آبی غلیظ که جذب کننده رطوبت است ، تغذیه می شود. دلیل این که از کلرات فلزات قلیایی معمولا استفاده نمی شود، خطرناکی خشک کردن محلول علیة این مواد است . کلرات ها می توانند مستقیما هیدروژن ایجاد شده در عملیات و آهن دوظرفیتی را اکسید کنند . واکنش اکسیداسیون کلی به شکل زیر اسـت :












